常言道:「預防勝於治療」,這雖是一句再平常不過的俗話,但畢竟確實力行的人屬少數,直到經歷了世紀大疫情-COVID-19的全球大流行,並造成近700萬人死亡的衝擊,近四年來,已養成了臺灣人人罩不離身的習慣以免於染疫的風險,各類傳染性疾病的疫苗施打率亦因此大幅提升,顯見大家對於預防保健的健康意識抬頭。目前的醫療對於疾病仍以治療為主,若能對可預知的危險進行事前的預防措施,不但可大大地降低醫療支出成本,患者亦能從中受益,免於受到病痛的折磨,或徒增死亡的風險。
一、造血幹細胞移植可治癒絶症,但療效受GvHD影響造血幹細胞移植 (hematopoietic stem-cell transplantation, HSCT)是許多血液系統惡性腫瘤及許多其他疾病最有效的治療方法1,在長達60多年的技術發展歷史下,移植的幹細胞來源已從骨髓擴充至週邊血或臍帶血,此外,開發出較低強度的預處理方案使適用範圍擴大到老年患者或患有合併症的患者,HSCT的突破技術已挽救了許多面臨絕症患者的生命,並改善了患者的生活品質。
然而,移植物抗宿主疾病(Graft versus Host Disease, GvHD)是幹細胞移植後最常見的嚴重併發症,會導致皮膚、肝臟和腸胃道的器官/組織損傷,嚴重影響移植後患者的生活品質及長期生存率,超過10%的患者會死於這種併發症,特別是異體幹細胞移植(allogeneic stem cell transplantation, allo-HSCT)技術的發展,可擴大來自於親人或是骨髓庫配對合適的捐贈者進行移植,帶來了更多治療癌症和免疫系統疾病的機會,然而,卻使得GvHD的問題更為突出,增加了患者發病及死亡的風險,是異體幹細胞移植成功的主要障礙。
二、什麼是移植物抗宿主疾病(GvHD)?GvHD是指異體幹細胞移植後,可能出現的多重器官症候群。當從捐贈者的移植物移植到患者(宿主)的T細胞將宿主的細胞識別為「外來細胞」時,T細胞被活化進而攻擊患者的細胞,就會引發移植物抗宿主反應,產生一系列的臨床綜合症,包括皮膚疹、腹瀉、腹痛、腸道蠕動停止、食慾不振、體重減輕、肝毒性及肝功能衰竭等症狀。患有GvHD的患者容易感染,遭受極大的痛苦,生活品質極差,更是異體幹細胞移植患者的主要死因2。
GvHD主要分為急性(acute graft-versus-host disease, aGvHD)和慢性(chronic graft-versus-host disease, cGvHD)兩種。過去HSCT後100天之內出現症狀被歸類aGVHD,而100天後出現症狀則歸為cGvHD。目前則改以根據2014年美國國家衛生研究院(National Institute of Health, NIH)提出之共識標準3,以臨床表徵和病理特性進行綜合判斷,在原本以100天為分界及特有症狀歸為「典型aGvHD」及「典型cGvHD」兩類之外,針對具典型aGvHD症狀,在移植100天後未達cGvHD特徵之診斷標準,或是100天後才出現典型aGvHD症狀,歸類為「持續性、復發性或遲發性aGvHD」,另一類則是兼具aGvHD與cGvHD特徵之「重疊綜合型GvHD」(圖1)4。
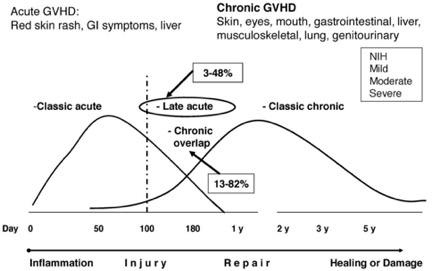
急性GvHD可根據嚴重程度分為I(輕度)、II(中度)、III(重度)和IV(非常嚴重)四級,主要依據皮膚、腸胃道、肝臟之血清膽紅素等臨床症狀進行分級。I 級較不影響患者預後,常不認為具有臨床重要性,因此,大多數研究集中於II-IV級和嚴重的III-IV級,發生 IV 級的患者預後特別差,死亡率接近 90%。
儘管目前GvHD的防治措施不斷優化,但仍有40%~60%的HSCT患者發生不同程度的aGvHD,亦有約30~70%的患者會出現cGvHD。
三、平衡GvHD的優缺點Mathé 等人於1965 年發表一位患有急性白血病患者接受了全身放射線照射(total body irradiation, TBI)後,進行親屬的骨髓移植,最終死於免疫併發症(最初稱為繼發性疾病,即為目前所稱之GvHD),但發現病患的白血病處於緩解狀態,顯示 GvHD 可導致白血病腫瘤細胞的清除,Mathé 因此創造了「移植物抗白血病」(graft-versus-leukemia, GvL)效應這個術語來描述此現象5。
雖然GvHD的症狀十分複雜多樣,並且難以應付,甚至可能嚴重到危及生命,但患有輕度 GvHD 可能是一件好事,來自捐贈者移植的T細胞雖因將患者體內的細胞視為外來物而引起GvHD,但亦同時具有防止感染及可攻擊並清除患者體內剩餘的癌細胞之功能,因此,根據統計,患有GvHD的HSCT患者復發率較低。
四、預防勝於治療總而言之,HSCT帶給許多罹患絕症的病患及家屬一線生機,但伴隨移植所產生的GvHD併發症對生活品質、移植成功率影響甚鉅,因此,透過有效的GvHD預防措施,以最大程度地降低GvHD的發生,為患者提供更有效、安全的醫療。
首先,GvHD的預防可以提高HSCT治療的成功率。當患者接受異體造血幹細胞移植前接受有效的預防措施,降低GvHD的發生率,這對於患者的康復和生存率至關重要,特別是對於已無藥可醫而需仰賴造血幹細胞移植的癌症患者。
其次,GvHD的預防有助於改善病患生活質量。GvHD所伴隨的多重臨床症狀,帶給患者極大的身體不適和心理壓力,有效的預防措施有助於減緩這些症狀的發展,提高患者的生活品質,使其更能夠應對治療過程中的種種挑戰。
此外,GvHD的預防有助於降低治療相關的併發症。GvHD不僅會對患者的免疫系統造成嚴重損害,還會增加感染和其他併發症的風險。透過預防GvHD,可以減少這些併發症的發生,提高患者治療過程的安全性。
預防GvHD是一個綜合性、重要的議題,醫學研究和臨床實踐的進展應不斷推動著預防措施的創新,提供患者更有效、更安全的治療選擇以造福群眾。
參考資料:
- N Granot et al., “History of hematopoietic cell transplantation: challenges and progress. “ Haematologica. 2020; 105(12): 2716-2729.
- A D'Souza et al., “Current Use of and Trends in Hematopoietic Cell Transplantation in the United States.“ Biol Blood Marrow Transplant. 2020; 26(8): e177-e182.
- MH Jagasia et al., “National Institutes of Health Consensus Development Project on Criteria for Clinical Trials in Chronic Graft-versus-Host Disease: I. The 2014 Diagnosis and Staging Working Group Report.” Biol Blood Marrow Transplant. 2015; 21(3): 389-401
- SZ Pavletic et al., “Are we making progress in GVHD prophylaxis and treatment?” Hematology Am Soc Hematol Educ Program. 2012; 2012: 251-264.
- HM Vriesendorp et al., “History of graft-versus-host disease.” Exp Hematol. 2016; 44(8): 674-688.